Уже на протяжении нескольких лет длятся патентные споры об использовании технологии CRISPR, позволяющей вносить изменения в ДНК и РНК. В этой статье мы рассмотрим спор между изобретателями данной технологии Институтом Броуд («Броуд») и Калифорнийским университетом в Беркли («Беркли»). Перед тем как перейти к изложению юридической сути спора, давайте разберемся, что же все-таки означает эта загадочная аббревиатура CRISPR/Cas9.
Что такое CRISPR, Cas9 и причем здесь белки?
«CRISPR» расшифровывается как Clustered Regularly Interspaced Short Palindromic Repeats (кластерные регулярно расположенные короткие палиндромные повторы). Это специализированная область ДНК с двумя отличительными характеристиками: наличие нуклеотидных повторов и так называемых «спейсеров». Повторяющиеся последовательности нуклеотидов – строительных блоков ДНК – распределены по всей области CRISPR. Спейсеры – это кусочки ДНК, которые разбросаны между этими повторяющимися последовательностями.
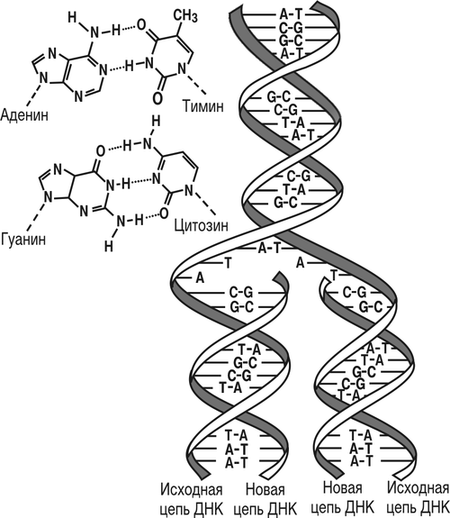
Например, у бактерий спейсеры образовались вследствие встреч с вирусами, ранее атаковавшими организм. Таким образом, спейсеры служат банком воспоминаний, который позволяет бактериям распознавать уже знакомые вирусы и отражать будущие атаки.
Если говорить простым языком, геномы различных организмов шифруют серию сообщений и инструкций в своих последовательностях ДНК. Редактирование генома заключается в изменении этих последовательностей за счет внесения разреза или разрыва в цепь ДНК и «прикрепления» желаемых последовательностей, в результате чего происходит «обман» естественных механизмов восстановления ДНК клетки.
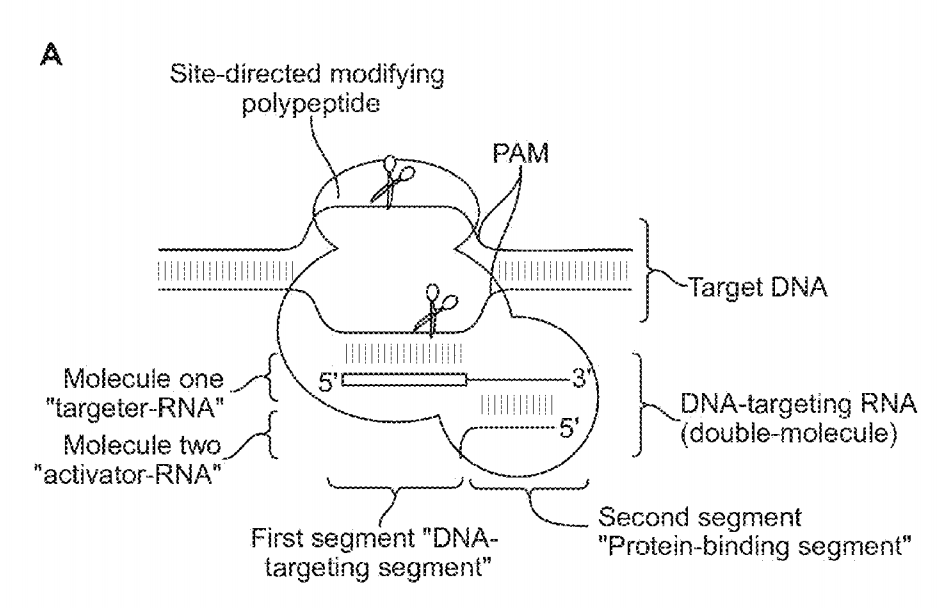
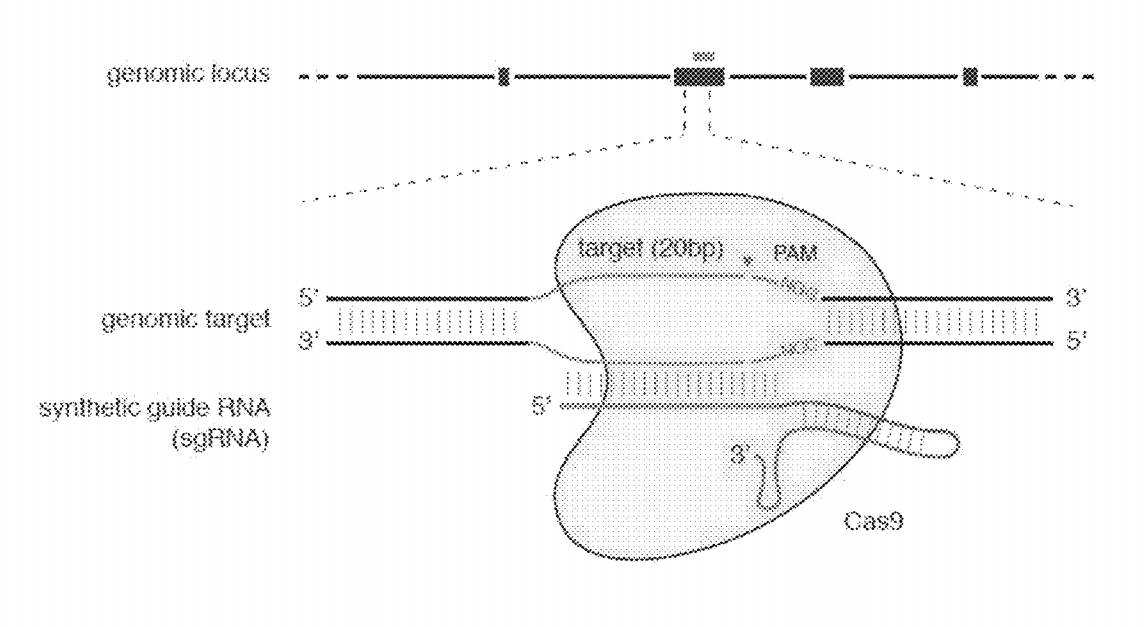
Cas9 (CRISPR associated protein 9, CRISPR-ассоциированный белок) – это белок особой группы, который присутствует у ряда бактерий и является частью адаптивной иммунной системы. То есть Cas9 запоминает определенные «враждебные» последовательности и в случае их обнаружения разрезает, словно ножницами, чужеродную ДНК. Ученым удалось с помощью РНК направить Cas9 и разрезать определенный, заранее известный ученым, участок ДНК для последующего точечного редактирования. Данное описание механизма CRISPR/Cas9 сильно упрощено; если вы заинтересованы в более научном описании, то далее вы можете обратиться к статье авторов данного механизма.
Предыстория патентного спора
Предысторию можно начать с начала 2011 года, когда изобретатель из Броуда доктор Фэн Чжан начал разработку систем CRISPR, которые могли успешно функционировать в эукариотических клетках. Это важный момент, и для наглядности мы далее расскажем, чем отличаются прокариотические клетки от эукариотических.
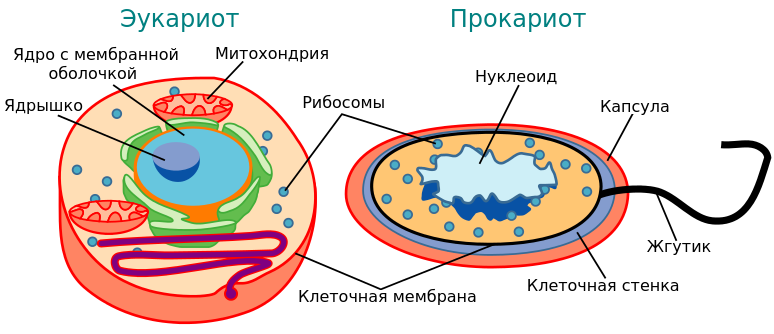
Эукариотические клетки (эукариоты) – это сложноструктурированные клетки животных (в том числе и людей), растений, грибов и т.д., основным отличием которых является сложное строение органов и наличие ядра.
Прокариотические клетки (прокариоты) – эти клетки были первыми живыми организмами, появившимися на Земле, они имеют простое строение их еще называют доядерными, так как они являются эволюционным предшественником эукариотов (ядерных клеток).
Клетки эукариоты в среднем намного крупнее прокариотических, разница в объёме может достигать тысячи раз, к тому же эукариоты включают около десятка видов различных структур, не характерных для прокариотов.
12 декабря 2012 года доктор Чжан подал свою первую патентную заявку на изобретение № 61/736,527, и тем самым был вынужден издать меморандум, раскрывающий многочисленные применения сконструированной формы системы CRISPR/Cas9, которая функционировала именно в эукариотических клетках. Так как выдача патента занимает достаточно большое количество времени, различные ученые успели ознакомиться и воспользоваться работами доктора Чжана. То есть в течение трех лет патентная заявка Чжана привела к выдаче десятка патентов в США, касающихся систем CRISPR/Cas9, разработанных для использования в эукариотических клетках.
Летом 2012 года доктор Чжан продолжал серию успешных экспериментов с системами CRISPR в эукариотических клетках. В то время как изобретатели из Беркли, среди которых были Дженнифер Дудна и Эммануэль Шарпантье, опубликовали статью под руководством Мартина Джинека с результатами своих экспериментов механизма CRISPR. В этой статье высказывались предположения о возможности того, что система CRISPR может быть альтернативой двум другим системам расщепления ДНК в эукариотических клетках. Однако эксперименты in vitro, представленные в статье, в определенной среде пробирки не дали никаких указаний относительно того, как можно спроектировать CRISPR для функционирования в эукариотических клетках.
Исследователи в лице членов правления Беркли и Броуда разработали и запросили патент для аналогичных методов редактирования генов с использованием технологии CRISPR. В мае 2012 года Беркли подал предварительную заявку на патент 13/842,859, добиваясь патентной защиты методов расщепления ДНК с использованием CRISPR без ссылки на конкретный тип клеток (эукариоты/прокариоты) или среду. Броуд подал заявку на патент чуть позже – в декабре 2012 года и, в отличие от Беркли, ограничил использование CRISPR эукариотическими клетками.
Благодаря процедуре ускоренного рассмотрения Ведомство по патентам и товарным знакам США («USPTO») одобрило заявку Броуда в 2014 году и выдало патент № 8,889,356, в то время как заявка Беркли все еще находилась на рассмотрении.
Стоит упомянуть о том, что до марта 2013 года в США действовала система «first-to-invent», которая предполагала, что в патентных спорах необходимо выяснять, кто первый изобрел технологию, а не кто первый формально подал заявку на патент. Теперь же в США используется система «first-to-file», которая отдает приоритет тому, кто первый подал заявку на выдачу патента. USPTO решило руководствоваться в данном споре принципом «first-to-invent», так как он действовал на момент подачи заявок.
Впоследствии Совет по патентным спорам и апелляциям («PTAB») выдал Броуду одиннадцать дополнительных патентов, связанных с технологией CRISPR. В 2017 году Беркли начал процедуру вмешательства (возражения) в PTAB, чтобы установить, совпадают ли изобретения Беркли и Броуда, и если да, то какая из сторон была первой в изобретении инструмента редактирования генов CRISPR. Процесс включал анализ заявки Беркли от 2012 года и двенадцати выданных Броуду патентов CRISPR, а также одной заявки, находящейся на рассмотрении.
Суть спора
Данная тема не является самой простой, но для большего понимания основной проблемы необходимо обратиться к критериям на выдачу патента, применяемым в США.
Суть спора заключается в том, что Броуд получил патент, который охватывает применение механизма CRISPR/Cas9 только в эукариотических клетках. В то время как Беркли подали заявку на патент раньше и указали на применение механизма CRISPR/Cas9 в прокариотических клетках, что является более широкой категорией. Тем самым начался спор о признании патента.
В США для соответствия патентоспособности идея должна пройти трехкомпонентный тест новизны, неочевидности и полезности. Кроме того, изобретение не должно находиться в публичном использовании или продаже в США более одного года до даты подачи заявки на патент. Патентный статут США гласит, что изобретение считается очевидным, «если разница между объектом, на который запрашивается патент, и известным уровнем техники такова, что объект в целом был бы очевиден для человека, имеющего обычные навыки в данной области, к которой относится предмет».
В разбирательстве 2017 года Броуд утверждает, что в статье Беркли под руководством Джиннека от 2012 года нет ни одного упоминания эукариотических клеток. К тому же в интервью после опубликования статьи профессор Дженнифер Дудна говорит о том, что способ применения в эукариотических клетках еще не выработан. Также заявка Беркли на патент не содержит ни одного упоминания ни о прокариотических, ни о эукариотических клетках. Патентная заявка содержит ряд технических новшеств, которые внесли в формулу ученые Броуда.
Беркли, в свою очередь, утверждает, что переход от прокариотов к эукариотам является очевидным продолжением их научного исследования от 2012 года, логично ведущего к охвату заявленного патента:
«Существенные различия между прокариотическими и эукариотическими клетками проистекают из эволюционного расхождения 1,5 миллиарда лет назад. С течением времени эукариотические клетки становились все более сложными и в конечном итоге образовывали многоклеточные организмы, тогда как прокариотические клетки оставались простыми одноклеточными организмами».
В качестве доказательства Беркли указывает ссылки технического характера на то, что Броуд использовал классические (общеизвестные) компоненты формулы, не привнося в формулу никакой научной новизны.
После вынесения решения PTAB Беркли направил жалобу в Апелляционный суд США по Федеральному округу. Рассмотрев дело, суд постановил, что заявка Броуда никак не входит в конфликт с предыдущей заявкой Беркли, так как не уточнено, к каким именно клеткам относится технология Беркли. Иными словами, из-за того, что Беркли не уточнил, в каких именно клетках применяется технология CRISPR, патент на применение в эукариотических клетках стоит оставить за Броудом, а все остальные области применения закрепить за Беркли.
Первое патентное притязание подтвердило, что патенты Броуда были выданы надлежащим образом на основании решения Апелляционного суда США по Федеральному округу от 10 сентября 2018 года. Апелляционный суд постановил, что претензии на патент Броуда к методам, используемым в эукариотических клетках, таким как редактирование генома, очевидно отличны и не могут быть разумно ожидаемы на основании результатов биохимических экспериментов в «пробирке».
В своих документах Беркли попытался избежать какой-либо оценки того, кто на самом деле первым изобрел метод, потому что все доказательства ясно показывают, что Беркли не был первым, кто изобрел какой-либо метод использования CRISPR в эукариотических клетках. Вместо этого Беркли до сих пор стремится убедить PTAB отменить предыдущие решения и, исходя из тех же данных, прийти к противоположному выводу, а именно, что успешные эксперименты на эукариотических клетках никогда не были необходимы.
Основным аргументом Броуда было утверждение о том, что CRISPR/Cas9 не следует сравнивать с существующими методами редактирования генов, такими как особые нуклеазы иных методов редактирования, в отличие от CRISPR/Cas9, который в природе активен только у прокариотов. Два других метода были известны своей способностью быть естественно активными в эукариотических системах. Вместо этого, как утверждает Броуд, CRISPR/Cas9 следует сравнивать с другими только прокариотическими регуляторными системами, такими как «рибопереключатели, рибозимы и интроны группы II», ни одна из которых не была использована особенно успешно в эукариотических клетках. Следовательно, был поднят один из основных вопросов спора: если механизм CRISPR/Cas9 не сработал у эукариотов, почему квалифицированный специалист мог ожидать, что CRISPR сработает у прокариотов?
В сентябре 2018 года Апелляционный суд США по Федеральному округу оставил в силе ранее вынесенные постановления о том, что патенты Броуда, выданные USPTO относительно редактирования CRISPR геномов эукариот, не противоречат патентным заявкам, поданным Беркли. PTAB описал важные различия между работой Броуда и Беркли:
«Броуд предоставил достаточные доказательства для подтверждения исследований, ограниченных системами CRISPR/Cas9 в эукариотической среде. Таким образом, эти исследования не связаны с изобретением Беркли, которое направлено на использование механизма CRISPR/Cas9 без ограничений на используемую среду. В частности, предоставленные доказательства показывают, что изобретение таких механизмов в эукариотических клетках не было бы очевидным по сравнению с изобретением механизма CRISPR/Cas9 в любой среде, включая прокариотические клетки или in vitro (в пробирке), поскольку специалист в данной области не мог бы обоснованно ожидать, что система CRISPR/Cas9 будет успешно функционировать в эукариотической среде. Этот факт показывает, что претензии сторон не пересекаются. Соответственно, следует прекратить патентный спор».
Подводя итог, патенты Броуда предназначены для редактирования генома и использования в эукариотических клетках, включая клетки животных, людей и растений, в то время как патенты Беркли не относятся к конкретным применениям в эукариотических клетках. Патенты Беркли и большая часть его заявок основаны на первоначальных заявках 2012 года, основанных на результатах экспериментов в пробирках (а не в эукариотических клетках, что важно, так как они не доказывают использование в эукариотических клетках).
PTAB подтвердил, что инновации Броуда явным образом подлежат патентованию. Это решение было поддержано Апелляционным судом Федерального округа США в октябре 2018 года.
Однако в 2019 году PTAB возобновил спор, объявив о новом патентном вмешательстве в отношении патентов CRISPR, принадлежащих обеим сторонам. Тем самым споры продолжаются и по сей день.
Итоги
Данная статья призвана прояснить процессуальные этапы патентных споров и описать технологию CRISPR/Cas9. Редактирование генома представляет чрезвычайно перспективное направление для развития науки и всего человечества. Подтверждением перспективности открытий в области геномного редактирования может послужить признание мирового сообщества, особенно после присуждения Нобелевской премии по химии двум ведущим ученым в этой области Дженнифер Дудне и Эммануэль Шарпантье.
Закрытая рассылка о праве и сделках в эпоху технологического суверенитета
Подписаться.webp)
.webp)